Le sfide nella produzione e iniezione di radiofarmaci marcati con Gallio-68 e le soluzioni Comecer
Traccianti a base di Gallio-68 sono sempre più spesso utilizzati nei reparti di Medicina Nucleare in Europa e nel mondo, sia per esami PET/CT nello lo studio di tumori neuroendocrini, sia per esami legati allo studio dei ricettori per somatostatina.
Questa tendenza si deve alla flessibilità del Gallio-68 nel tipo di legami chimici, alla disponibilità di generatori 68Ge/68Ga e a un buon rapporto tra la dose somministrata e i tempi di decadimento.
Negli ultimi 4 anni il numero di pubblicazioni scientifiche sull’argomento è aumentato esponenzialmente, così come il numero di pazienti trattati con questo tipo di radiofarmaci. La pubblicazione di monografie nella Farmacopea Europea e la presenza di “market authorization” per alcuni generatori di 68Ga stanno abbattendo le barriere che rendevano complessa l’implementazione di questo radio-tracciante nelle preparazioni routinarie.
È probabile quindi che questo trend positivo nell’uso routinario del 68Ga continui e sia destinato ad aumentare nei prossimi anni.
Rimangono però alcune criticità che potrebbero ostacolare la diffusione di questo radiotracciante: in primis, la produzione di Gallio-68 richiede di implementare processi di preparazione con moduli di sintesi automatica, richiede sistemi di Controllo Qualità più complessi di quelli che si trovano abitualmente in piccoli contesti di Medicina Nucleare ospedaliera e comporta una gestione del flusso di lavoro “sintesi e dispensazione” all’interno di celle calde rispettando le “norme di buona preparazione”, siano esse nazionali o europee.
La necessaria premessa è che la produzione di radiofarmaci marcati con Gallio-68 è influenzata da molteplici fattori. La sintesi viene integrata in un contesto ospedaliero che cambia di volta in volta, a seconda di come viene gestito il rischio farmaceutico e di come vengono interpretate le norme di preparazione. Da questo punto di vista, soluzioni diverse possono risultare ugualmente adeguate. Tuttavia, le linee guida GMP stanno entrando anche in queste realtà, e porteranno, nel tempo, gli enti regolatori e le agenzie di controllo a uniformare i requisiti del processo sviluppato in ambito ospedaliero a quelli del processo sviluppato nell’ambito delle radiofarmacie centralizzate.
Come si traduce questo approccio nella realtà operativa, e che tipo di investimento implica nelle attrezzature di manipolazione e preparazione per chi vuole introdurre l’uso di questo radioisotopo nelle proprio attività routinarie?
Per capirlo prima di tutto va analizzato come questo isotopo entra nel reparto ospedaliero oggi e come potrebbe farlo in futuro. Esistono infatti diverse vie:
- Attraverso un generatore di 68Ge/68Ga
- Attraverso l’acquisto di un farmaco già marcato e distribuito da una farmacia centralizzata
- Attraverso la produzione interna da ciclotrone
Il primo punto oggi è preponderante, ma la possibilità di una distribuzione centralizzata soprattutto in vista di marketing authorization EU e FDA relativi ai 68Ga-DOTA-x (o altri) diventerà una possibilità concreta e fruibile nei prossimi anni. La produzione da ciclotrone, pur essendo solo agli inizi, gode invece delle potenzialità di diventare la più attraente dal punto di vista dei costi evitando l’acquisto dei generatori ed integrandosi all’interno del normale flusso di produzione di radiotraccianti da ciclotrone. Un esempio concreto è la recente tecnologia introdotta da IBA per la produzione di Gallio-68 da target liquido.
Una cella di manipolazione, sintesi o dispensazione deve perciò tenere conto di tutti e tre questi aspetti se si intende procedere ad un investimento che abbia un valore per gli anni futuri.
Definito come il Gallio-68 arriva nel reparto di Medicina Nucleare si possono valutare le metodologie operative che lo porteranno fino alla fase finale di trattamento del paziente.
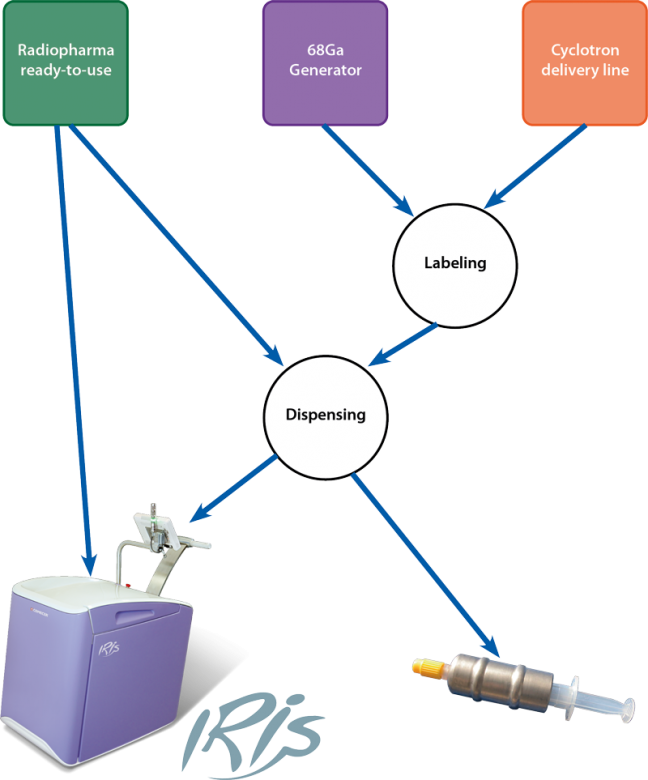
Trascurando la fase dei Controlli di Qualità che comunque non potrà mancare a meno di farmaci venduti sotto marketing authorization, il trattamento del paziente può avvenire in due modi: tramite iniezione con siringa tradizionale preparata in area asettica, oppure tramite un sistema di iniezione automatico come il nostro iniettore multidose IRIS, in grado di iniettare anche isotopi come il Gallio-68 e non solo il Fluoro-18.
Con il sistema IRIS è possibile bypassare le fasi di preparazione e labeling utilizzando un flacone multidose pronto all’iniezione distribuito da una farmacia centralizzata. Il flusso operativo sarebbe dunque identico a quello che oggi molti siti impiegano per l’FDG.
L’IRIS può essere impiegato anche con un flacone multidose prodotto internamente. La sua applicazione riduce la radio-esposizione degli operatori durante il trasporto del radiofarmaco e durante l’iniezione. Inoltre, rende più veloce il flusso operativo di preparazione, dato che dalla cella calda vengono estratti solo il flacone multidose ed i flaconi di per i Controlli di Qualità. Non vengono per cui manipolate siringhe.
Quando la produzione parte dal generatore di Gallio-68, ovvero ad oggi nella maggior parte dei casi, vi sono due possibili flussi di lavoro, estremamente diversi a livello normativo. Questi flussi richiedono tipologie diverse di celle calde poiché richiedono diversi tipi di aree classificate.

Nel primo caso, il generatore, il modulo di sintesi ed il dispensatore (se presente) sono installati in un singolo vano schermato e classificato, mentre nel secondo caso in vani distinti e separati.
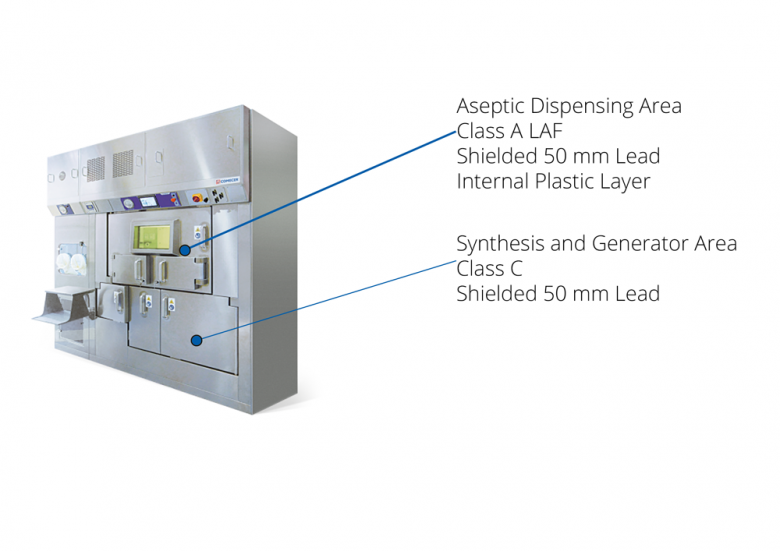
Per il labeling del 68Ga non è possibile utilizzare “cold kit” (anche se su questo aspetto è probabile che entreranno delle novità sul mercato nei prossimi anni) ed è necessaria una fase di eluzione dal generatore con soluzione di HCl e sistemi di pompaggio molto più complessi di quello che avviene sui generatori di 99mTc. Queste operazioni sono quindi considerate ad “alto rischio microbiologico” a livello normativo, e viene spesso imposto dagli enti locali l’uso di un isolatore in classe A LAF (con flusso laminare) per processi asettici.
Non viene per cui accettato in molti paesi l’uso di cappe in classe A. A livello radioprotezionistico è inoltre un scelta anche che tutela maggiormente l’operatore: la cappa infatti per sua natura offre una schermatura parziale. Essendo il Gallio-68 un isotopo per indagini PET e avendo anche componenti ad alta energia nello spettro di decadimento, la sua preparazione è critica dal punto di vista della protezione dell’operatore dalle radiazioni ionizzanti.
Per questo motivo, unito all’aspetto normativo, l’isolatore in Classe A rimane la prima scelta per questo tipo di processo.
La classificazione GMP dell’area di lavoro in Classe A è un vincolo su due fronti: pone infatti limiti precisi sia sul particolato che sulla presenza di contaminazione microbiologica. Inoltre, la Classe A è solo uno dei requisiti che fanno parte di una richiesta più ampia ovvero della necessità di eseguire un processo asettico. Sarebbe quindi più corretto dire che è necessario dotarsi, non solo di una “cella in classe A”, ma di un sistema che permetta di implementare un processo asettico nel suo complesso.
Questo pone diverse implicazioni, la più importante delle quali è la seguente: è possibile un processo asettico in un vano isolato in cui vengono posizionati contemporaneamente un sistema di sintesi automatico, un generatore di 68Ga, una serie di flaconi di waste, reagenti chimici, disposable complessi da spacchettare, un dispensatore, i contenitori finali e i relativi accessori?
Di certo è molto complesso, e forse difficilmente accettabile da un occhio attento alle normative. Come processo GMP non è sicuramente accettabile, tanto che è consolidata la necessità di separare sintesi e dispensazione nei processi produttivi di qualsiasi tracciante.
Spesso viene considerata la presenza di un “disposable chiuso” nel lato chimico come attenuante, in quanto essendo chiuso non ci sono possibili contaminazioni esterne. Ma questo approccio vede diversi punti critici:
- Il disposable è “chiuso” solo parzialmente
- Vengono comunque connessi flaconi e reagenti nella zona asettica
- Il disposable o i reagenti spesso non prevedono un approccio a doppia busta
- Sono presenti accessori dei moduli di sintesi non adatti alla classe A (come pompe)
- Sono presenti sacche con soluzioni di HCl che creano oltre ad un rischio puramente microbiologico, anche un rischio chimico nel composto finale. La dimostrazione, come verrà meglio spiegato in seguito, è la facile presenza di corrosione in questo tipo di celle caldo
- Il disposable e il modulo sono spesso difficilmente pulibili in profondità
- Il modulo di sintesi non è scontato possa essere sottoposto a processi di decontaminazione su base di VPHP
Se l’approccio normativo è già oggi difficilmente accettabile, separare i due ambienti rimane l’unica opzione sicura a lungo termine.

LE SOLUZIONI COMECER
Comecer, con la sua esperienza in campo radiofarmaceutico, offre soluzioni alla gestione del processo di produzione, manipolazione e dispensazione del prodotto, rispettando gli standard più elevati in termini di conformità alle norme, di usabilità e di investimento.
La proposta di Comecer prevede diverse tipologie di celle calde e dispensatori che possono permettere il flusso di lavoro descritto in questo articolo.
MUSA 68Ga: isolatore schermato in classe A, soluzione per media-bassa attività, compatto, portelli passaggio mani con guanti, produzione di siringhe o flacone multidose per IRIS

BBST-COMBO: isolatore schermato per sintesi e dispensazione (classe A), soluzione per alte attività, telepinze per dispensazione, produzione di flaconi o flacone multidose per IRIS

ELENA: Isolatore schermato in classe A, soluzione per media-bassa attività, alta ergonomia, portelli passaggio mani con guanti, produzione di siringhe o flacone multidose per IRIS
BBS: cella schermata per sintesi, soluzione per alte attività e produttività, deve essere collegata ad un isolatore schermato per dispensazione

Questa tabella di comparazione aiuta a valutare quale tipo di soluzione si adatta meglio alle proprie esigenze e necessità operative senza sacrificare i concetti discussi:
| CARATTERISTICA |
MUSA 68Ga |
ELENA |
BBST-COMBO |
BBS |
| Possibilità di due comparti separati, sintesi in Classe C e dispensazione in Classe A |
Si |
Si |
Si |
Solo sintesi |
| Possibilità di avere sintesi e dispensazione nello stesso comparto in Classe A |
Si |
Si |
No |
No |
| Caratteristica fondamentale della cella |
Compatta |
Alta ergonomia (larghezza area Classe A maggiorata e posizione del modulo di sintesi rialzata) |
Processi ad alta attività gestiti con telepinza |
Ottimale per la sintesi in grandi laboratori |
| Possibilità di inserire la cella in un processo GMP |
Si |
Si |
Si |
Si |
| Ideale per processi con beta emettitori come 177Lu e 90Y |
Opzionale
schermatura beta |
Inclusa
schermatura beta |
Non richiesta schermatura beta non essendoci manipolazioni dirette |
Non richiesta schermatura beta non essendoci manipolazioni dirette |
| Possibilità di doppio airlock in Classe B per inlet ed outlet materiali in Classe A |
Si |
Si |
Si |
Non richiesto |
| Sollevatore automatico in airlock per poter caricare (caso di ingresso del flacone madre) e scaricare (caso del flacone multidose) contenitori in piombo pesanti con facilità e con la massima ergonomia |
Si |
Si |
Non richiesto |
Non richiesto |
| Area di sintesi in grado di ospitare uno o più generatori 68Ge/68Ga |
Si |
Si |
Si |
Si |
| Numero di generatori installabili |
2 |
2 |
2 |
2 |
| Connessione con eventuale linea per ciclotrone |
Opzionale |
Opzionale |
Presente |
Presente |
| Possibilità di protezione anti-corrosione |
Si |
Si |
Si |
Si |
| Restrizioni nella tipologia di moduli installabili dovute alle dimensioni |
Necessaria valutazione |
Necessaria valutazione |
Area adatta per grandi moduli di sintesi |
Area adatta per grandi moduli di sintesi |
| Possibilità di prevedere HPLC di corollario al modulo |
No |
Solo se installato in Classe A |
Si |
Si |
| Dispensatori suggeriti per siringhe |
FEBO |
FEBO |
FEBO |
Necessaria cella di dispensazione |
| Dispensatori suggeriti per flacone |
ARGO |
ARGO |
ARGO |
Necessaria cella di dispensazione |
| Ideale per la produzione di flacone multidose impiegabile per IRIS |
Si |
Si |
Si |
Necessaria cella di dispensazione per QC |
La protezione anti-acido è ritenuta una importante opzione, dato che è stato evidenziato in diverse strutture ospedaliere e radiofarmacie come l’eluizione del generatore con soluzioni di HCl, la dinamica della sintesi ed eventuali piccoli errori commessi dagli operatori, siano in grado di innescare processi di corrosione anche di acciai farmaceutici come l’AISI316L usato comunemente nei nostri isolatori.
I processi di corrosione sono recuperabili, ma innescano problematiche sia a livello di cella calda, sia a livello farmaceutico. Per questo, la proposta di Comecer prevedere sempre la possibilità di implementare contromisure efficaci contro la corrosione delle pareti interne delle celle calde.
Inoltre viene considerato che il labeling con peptidi del Gallio-68 si affianca spesso al labeling con Lutezio-177 e Ittrio-90. I moduli di sintesi infatti affrontano questi isotopi con gli stessi processi chimici ed a volte lo stesso disposable. Diviene per cui necessario, per mantenere massima la flessibilità e sicurezza della soluzione, prevedere schermature per beta emettitori come nelle celle di manipolazione MUSA 68Ga ed ELENA.
Il 68Ga infatti si affianca a terapie a base di 177Lu e 90Y. Per questo motivo la gestione del flusso di preparazione deve tenere conto che sempre più spesso l’uso del 68Ga per la diagnosi è propedeutico al successivo trattamento terapeutico a base di beta emettitori. Una cella calda dotata di queste caratteristiche è dunque ideale sia per il 68Ga preso singolarmente sia per quelle procedure che vengono indicate con la parola “teragnostiche”.
In conclusione Comecer propone sul mercato prodotti che intendono garantire la loro usabilità nel tempo e siano in grado di affrontare gli aspetti normativi non solo considerando le richieste attuali, ma anche preparandosi a quelle future. La flessibilità operativa e la capacità di adattarsi ai diversi tipi di processi nei trattamenti diagnostici o terapeutici, sono infatti la chiave per massimizzare l’investimento ed ottenere un risultato ottimale nel tempo.
Hai una domanda tecnica? Vorresti vedere l’IRIS dal vero senza impegno? Vuoi richiedere una quotazione? Compila il modulo sotto.







