Se connecter
Log InS’inscrire
L'enregistrement est destiné aux professionnels qui travaillent avec des technologies de confinement et d'isolation et il autorise un accès total à nos fiches de données et catalogues de produits
S’inscrire
La société faisant l’objet de cette étude de cas est une société multinationale opérant dans le secteur de la biotechnologie. Le plan d’investissement prévoit un nouveau laboratoire dédié à l’ingénierie tissulaire à des fins commerciales, conformément à la norme BPF. L’intention de construire une installation de pointe a amené la Société à étudier l’adoption de la technologie d’isolation afin de garantir la continuité complète d’un environnement de niveau A et d’assurer une meilleure qualité du produit final ainsi qu’une conformité totale aux réglementations BPF et FDA. Le défi consistait à développer des équipements de laboratoire personnalisés ainsi que des solutions spécifiques pour garantir l’asepsie tout en conservant la facilité d’utilisation et de fonctionnement.
La régénération des tissus humains est en large expansion et les champs d’application s’élargissent de jour en jour. Certains d’entre eux sont déjà bien établis dans les processus de fabrication, de sorte que les aspects liés à l’utilisation commerciale sont principalement liés à la mise à niveau du laboratoire, à la conformité réglementaire, à la rentabilité globale en termes de coût d’investissement et de coûts opérationnels. Les défis posés par la nécessité de niveaux élevés de stérilité et l’élimination de toute contamination croisée au sein de la médecine régénératrice (voir le livre blanc « les défis de la stérilité et de la contamination croisée en génie tissulaire et en médecine régénératrice ») poussent à l’adoption de la technologie d’isolation au lieu des salles blanches traditionnelles, car les avantages démontrés dans le traitement aseptique pour l’industrie pharmaceutique sont évidents.
Afin de mettre en œuvre une approche qualité par conception, la première chose était de définir avec la Société les conditions du processus en termes de :
Toutes les différentes étapes de la culture cellulaire impliquent des techniciens qualifiés qui suivent des protocoles spécifiques pour atteindre le produit final. En termes génériques, les étapes les plus importantes pour atteindre la confluence sont : l’élimination du surnageant, l’incubation, le détachement (pour la culture monocouche), l’observation et le comptage. Pour
l’entreprise, un certain niveau de flexibilité était également souhaité afin d’être prêt pour différentes techniques et produits. L’équipement suivant a été nécessaire pour être disponible tout au long du processus :
Les cellules primaires peuvent atteindre le laboratoire dans des conditions et des emballages différents, tandis que tous les autres consommables tels que les pipettes, les milieux de culture, les flacons, les sacs, le FBS, le bleu de trypan, la trypsine, etc. ont des récipients déjà utilisés par la Société.
La nécessité d’avoir une entrée et une sortie pour les consommables, pour les cellules primaires, pour la sortie du produit final et pour la manipulation des déchets et des outils a été donnée comme un must par la Société.
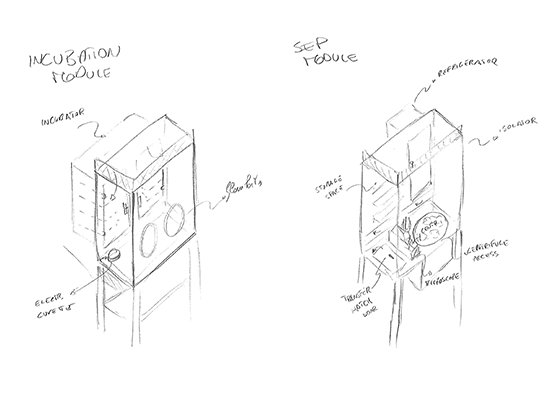
L’esquisse initiale a été créée en gardant à l’esprit à la fois le traitement aseptique général utilisé dans la technologie d’isolation (formulation, test de stérilité et finition de remplissage stérile) et les solutions d’intégration d’équipement dans le traitement API.
L’idée de séparer la zone technique non classifiée du côté opérateur est issue d’un concept développé dans le remplissage de flacons stériles appelé « design de balcon ». Les avantages offerts en termes de fonctionnement et d’entretien des isolateurs et des équipements intégrés sont bien reconnus par l’industrie pharmaceutique.
Sur le marché, il n’y avait pas d’incubateurs, de réfrigérateurs et de centrifugeuses qui pouvaient être intégrés dans des isolateurs comme nous l’avons voulu.
Pour permettre aux volumes internes de la centrifugeuse, de l’incubateur et du réfrigérateur d’être continus avec le boîtier isolateur de classe A (FDA – classe 100).
Cela devait être soumis aux cycles de décontamination par peroxyde d’hydrogène en phase vapeur pour atteindre une réduction de 6 log sur les spores bactériennes, ainsi que pour faire partie intégrante de l’enceinte en termes d’étanchéité à l’air. En outre, l’acier inoxydable 316L avec finition de nuance miroir devait être garanti dans tous les composants de volume interne lorsque cela était techniquement possible.
Deux modules ont été définis à cet effet, ainsi qu’une trappe de transfert pour le transfert de matériau :
La contrainte globale de l’espace de laboratoire a déterminé la taille de chaque module, tandis que la trappe de transfert a été maximisée dans les dimensions à 300x400x300 mm. En termes de fonctionnalité du processus, le diagramme ci-dessous représente ce qui était prévu pour chaque module :
Pour les caractéristiques de l’isolateur, la conception a été principalement guidée par BPF et ANSES en tant que principe de conception, ainsi que par les normes et directives de référence en matière de traitement aseptique au sein de la technologie d’isolation. À partir de cette évaluation, les caractéristiques techniques suivantes ont été définies comme nécessaires pour l’application de la Société :
La conception de l’intérieur de chaque module est la suivante :
La configuration de chaque unité d’isolation se compose d’un module de séparation avec deux modules d’incubation sur le côté, avec une trappe de transfert placée au bas du module de séparation pour desservir les trois modules.
Les solutions d’intégration sont représentées dans les images ci-dessous.
Le microscope a été équipé d’un appareil photo numérique connecté à un moniteur externe, la cuvette d’électroporation a été placée dans la chambre, tandis que le boîtier de commande est à l’extérieur.
Les isolateurs étaient équipés de tous les capteurs et sondes généralement nécessaires pour ce type d’application : un testeur d’intégrité des gants intégré, un anémomètre, un capteur de température et d’humidité relative, un manomètre pour le contrôle d’obstruction du filtre, une vérification automatique de l’intégrité des fuites avant le cycle de décontamination, etc.
La disposition finale de la suite de fabrication a prévu un côté de laboratoire classé comme classe D selon les BPF alors que le côté technique à l’arrière des isolateurs (nécessaire pour l’accès à la maintenance) n’est pas classé.
Par conséquent, les solutions d’intégration spécifiques développées dans le cadre de ce projet conduisent à leur mise en œuvre dans d’autres domaines de la médecine régénérative, tels que la thérapie cellulaire, la manipulation des cellules souches et le génie tissulaire.
Voir les solutions ATMP et de thérapie cellulaire et génique »
Connectez-vous à votre compte Comecer pour télécharger les fiches techniques
Log In Lost PasswordActualités et invitations à des événements et à des salons directement dans votre messagerie
S'inscrire
Technical

Statistical

Targeting